BPOM: Vaksin Merah Putih Segera Kantongi Izin Darurat COVID-19
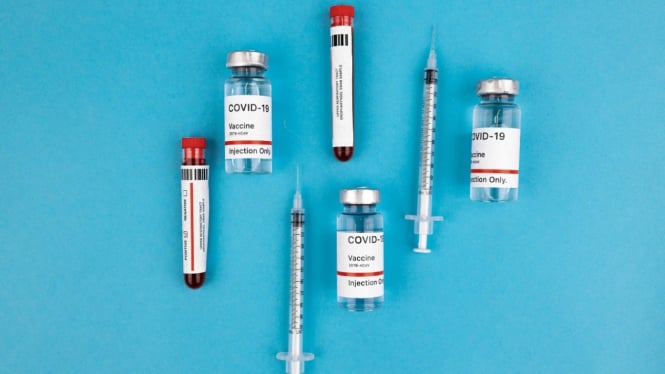
- Pexels/Maksim Goncharenok
VIVA Lifestyle – Vaksin Merah Putih tengah memasuki uji klinis fase tiga untuk mencegah COVID-19 yang kian bermutasi. Badan Pengawas Obat dan Makanan (BPOM) menuturkan bahwa uji klinis ini akan melibatkan sebanyak 4 ribu relawan.
Indonesia saat ini tengah mengembangkan Vaksin Merah Putih yang diprakarsai oleh berbagai institusi, mencakup akademisi dan lembaga penelitian seperti Lembaga Eijkman, Lembaga Ilmu Pengetahuan Indonesia (LIPI), Universitas Indonesia (UI), Institut Teknologi Bandung (ITB), Universitas Gadjah Mada (UGM), dan Universitas Airlangga (UNAIR).
Vaksin Merah Putih merupakan vaksin COVID-19 dengan platform inactivated virus, hasil kerja sama UNAIR dengan PT Biotis Pharmaceutical Indonesia (PT Biotis). Vaksin ini merupakan karya murni dari peneliti dan industri farmasi di Indonesia yang dikembangkan dari hulu atau awal tahapan pengembangan vaksin baru dengan menggunakan Virus SARS-CoV-2 yang diisolasi dari pasien COVID-19 di Surabaya.
Berikut fakta terkait vaksin COVID-19 Merah Putih buatan Indonesia.
Tenaga kesehatan mengangkat bendera Merah Putih dalam pelaksanaan vaksinasi COVID-19 pada pegawai pemerintah di Jakarta tahun lalu.
- ANTARA/M Risyal Hidayat
Segera Kantongi Izin Darurat
Kepala Badan POM RI, Penny K. Lukito bersama perwakilan dari Kementerian Kesehatan RI menghadiri Kick Off Uji Klinik Fase 3 Vaksin Merah Putih Unair – PT Biotis di Aula Fakultas Kedokteran Universitas Airlangga, Surabaya. Selain itu, turut hadir pada acara Kick-Off ini, yaitu perwakilan dari UNAIR, PT Biotis, dan Tim Peneliti Vaksin Merah Putih.
Dalam kesempatan ini, Kepala Badan POM menyampaikan apresiasi terhadap langkah yang dilakukan oleh Unair dan PT Biotis serta Rumah Sakit Umum Daerah Dr. Soetomo di Surabaya sebagai center pelaksanaan uji klinik.
Dalam proses pengembangannya, vaksin yang dikembangkan oleh UNAIR menjadi front runner dengan dimulainya uji klinik fase 3, yang artinya vaksin dapat segera digunakan setelah uji klinik fase 3 selesai dilakukan dan memperoleh Izin Penggunaan Darurat atau Emergency Use Authorization (EUA) dari Badan POM.
“Ini merupakan salah satu contoh implementasi kolaborasi triplehelix. Di mana akademisi (UNAIR) mengembangkan vaksin, pelaku usaha (PT Biotis) melakukan produksi skala masal, dan pemerintah (antara lain Badan POM dan Kementerian Kesehatan) mendukung pengembangan vaksin ini melalui pendampingan selama proses pengembangannya”, ujar Kepala Badan POM dengan bangga dalam sambutannya.
Kepala Badan Pengawas Obat dan Makanan Republik Indonesia (BPOM RI), Penny K Lukito.
- ANTARA FOTO/Fikri Yusuf
Rekrut 4 ribu Subjek
Uji klinik fase 3 direncanakan akan merekrut sebanyak 4.005 subjek uji dan akan dilaksanakan di center uji klinik Rumah Sakit Umum Daerah (RSUD) Dr. Soetomo, Surabaya dan 3 satellite sites, yaitu Rumah Sakit UNAIR, Surabaya; RSUD Dr. Saiful Anwar, Malang; dan Rumah Sakit Paru, Jember. Dalam tahap ini, uji klinik tidak akan menggunakan plasebo sebagai pembanding.
Dibandingkan Vaksin CoronaVac
Vaksin uji akan dibandingkan dengan Vaksin CoronaVac, yang telah mendapatkan EUA dari Badan POM dan masuk dalam Emergency Use Listing (EUL) WHO, serta mempunyai platform yang sama dengan Vaksin Merah Putih, yaitu inactivated virus.
Sebelumnya uji klinik fase 1 telah dimulai pada 8 Februari 2022 dan uji klinik fase 2 pada 28 Maret 2022. Saat ini, vaksin sedang dalam tahap pengamatan atau follow up setelah suntikan kedua.
Badan POM telah mengawal pengembangan Vaksin Merah Putih UNAIR ini sejak awal dengan memberikan asistensi melalui pertemuan yang dilakukan secara daring maupun luring. Asistensi ini diberikan kepada peneliti, dimulai dari pelaksanaan uji non-klinik pada hewan, dilanjutkan uji klinik pada manusia mulai dari fase 1, 2, dan tentunya fase 3 yang saat ini sedang dilaksanakan.
"Badan POM juga memberikan asistensi pemenuhan Cara Pembuatan Obat yang Baik (CPOB) kepada PT Biotis untuk persiapan produksi vaksin secara masal," lanjut Kepala Badan POM.
MUI mengeluarkan fatwa halal vaksin Merah Putih yang dikembangkan Unair
- MUI
Halal MUI
Pada 7 Februari 2022, Majelis Ulama Indonesia (MUI) telah mengeluarkan Fatwa Nomor 8 Tahun 2022 terkait kehalalan Vaksin Merah Putih yang berlaku hingga 6 Februari 2026. Hal tersebut merupakan kabar baik bagi kita semua, karena Vaksin Merah Putih merupakan Vaksin COVID-19 pengembangan dalam negeri pertama yang telah tersertifikasi halal.
Tentu saja, lanjut Kepala BPOM, itu sangat mendukung putusan Mahkamah Agung Nomor 31P/HUM/2022 atas rekomendasi untuk penyediaan vaksin halal dalam program vaksinasi nasional.
“Patut kita syukuri, pengembangan dari hulu ke hilir Vaksin Merah Putih tersebut dapat diselesaikan sampai memasuki uji klinik fase 3, sehingga diharapkan dapat mendukung kemandirian dalam pembuatan vaksin COVID-19 dalam negeri,” harapnya.
Dengan diterbitkannya Persetujuan Pelaksanaan Uji Klinik (PPUK) fase 3 Vaksin Merah Putih oleh Badan POM, tim peneliti dan sponsor, yaitu Kementerian Kesehatan, PT Biotis, dan UNAIR diharapkan senantiasa memenuhi semua ketentuan agar kemanfaatan hasil uji klinik dapat menjadi dasar keputusan yang baik bagi kepentingan peningkatan kesehatan masyarakat.